①此次印度尼帕病毒病聚集性疫情规模较小,尚未发现地区病例外溢的报道;
②本次资本市场相关行情本质上属于典型的事件驱动型题材炒作,仅部分环节具备短期业绩兑现基础。
《科创板日报》2月4日讯(记者 黄修眉)深圳核心医疗科技股份有限公司(下称:“核心医疗”)于近日回复了上交所下发的首轮审核问询。
回顾核心医疗上市进程,其是科创板第五套上市标准重启后,首家获受理的创新医疗器械企业。其科创板IPO申请于2025年11月6日获受理,上交所于同年11月21日下发首轮审核问询,并于2026年2月2日更新回复。
以植入量计算,核心医疗是我国最大人工心脏企业,手握全球最小、最轻量化人工心脏产品,在人工心脏这一市场需求巨大但技术壁垒高企的领域,其技术先进性、与全球范围内已获批产品异同、商业化路径与市场空间等,成为监管层与市场共同关注的话题。
另有三款产品或有望在全球范围内首发获批
《科创板日报》记者注意到,上交所在审核问询中首先关注的方面,是核心医疗人工心脏领域产品的技术先进性、临床价值和竞争力。
核心医疗表示,人工心脏领域产品研发技术壁垒较高,公司核心技术均为自主研发,Corheart® 6突破人工心脏小型化瓶颈,系目前全球体积最小、重量最轻的商业化磁悬浮植入式人工心脏。
从产品性能要求来看,植入式人工心脏的临床开发目标及趋势主要包括:小型化和轻量化、提升血液相容性、提高患者生存质量、扩展临床适用性、数字化和智能化;介入式人工心脏的临床开发目标及趋势主要包括:更小的产品尺寸下实现更高泵血流量、提高血液相容性、更长临床可支持时间、智能化控制。
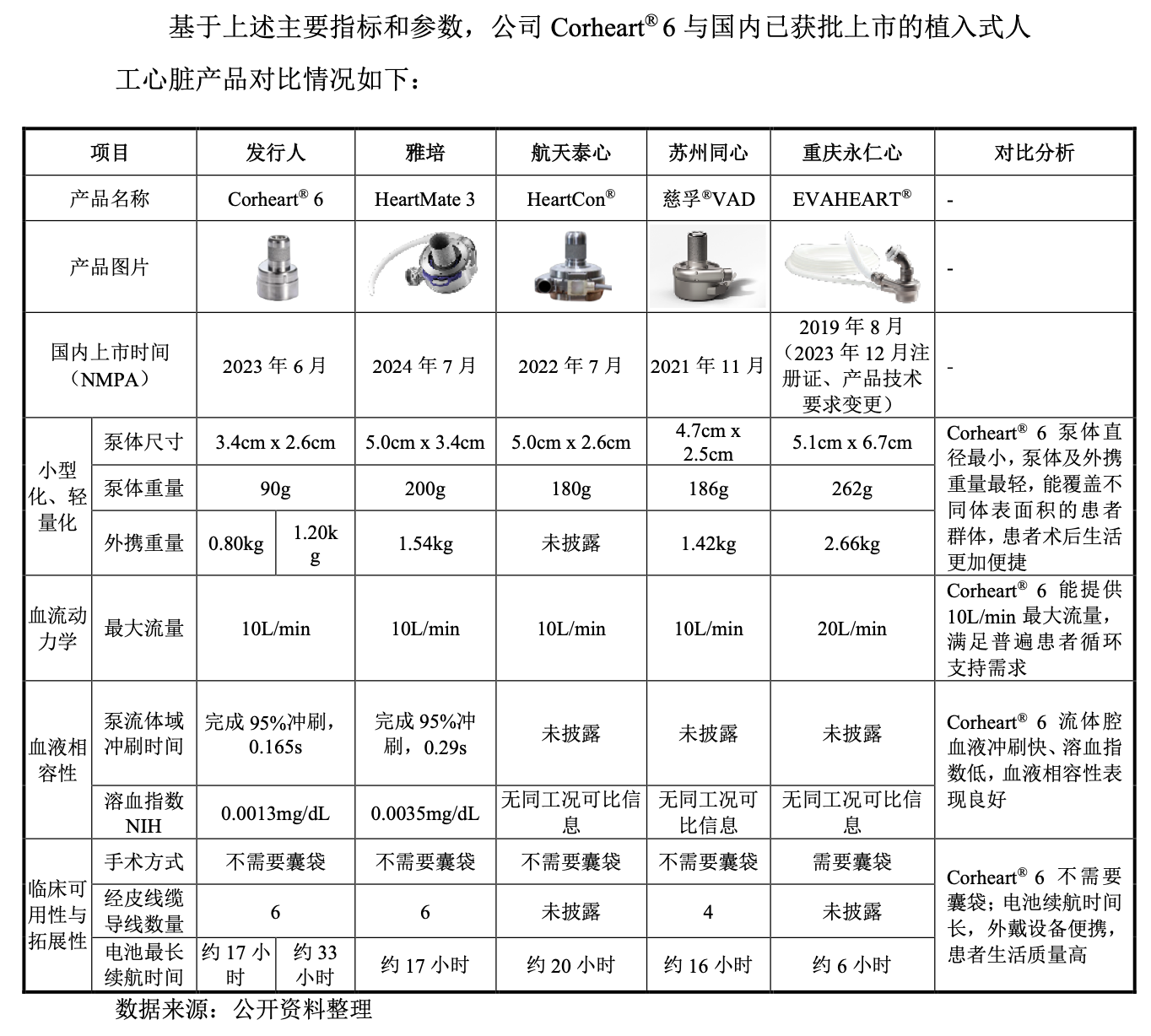
(图:植入式人工心脏Corheart®6与国内已获批上市的植入式产品对比分析)
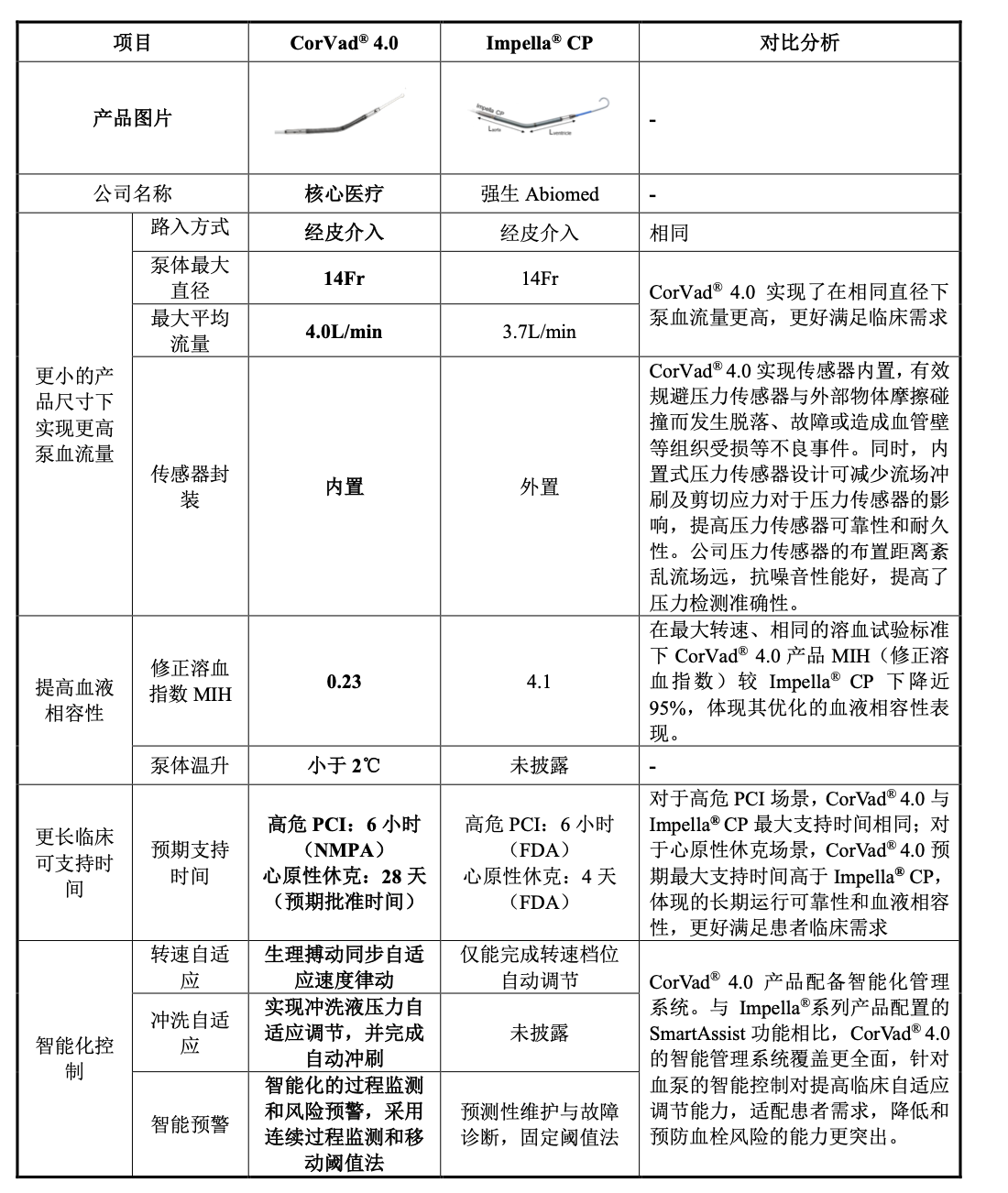
(图:介入式人工心脏CorVad® 4.0与Impella® CP对比分析)
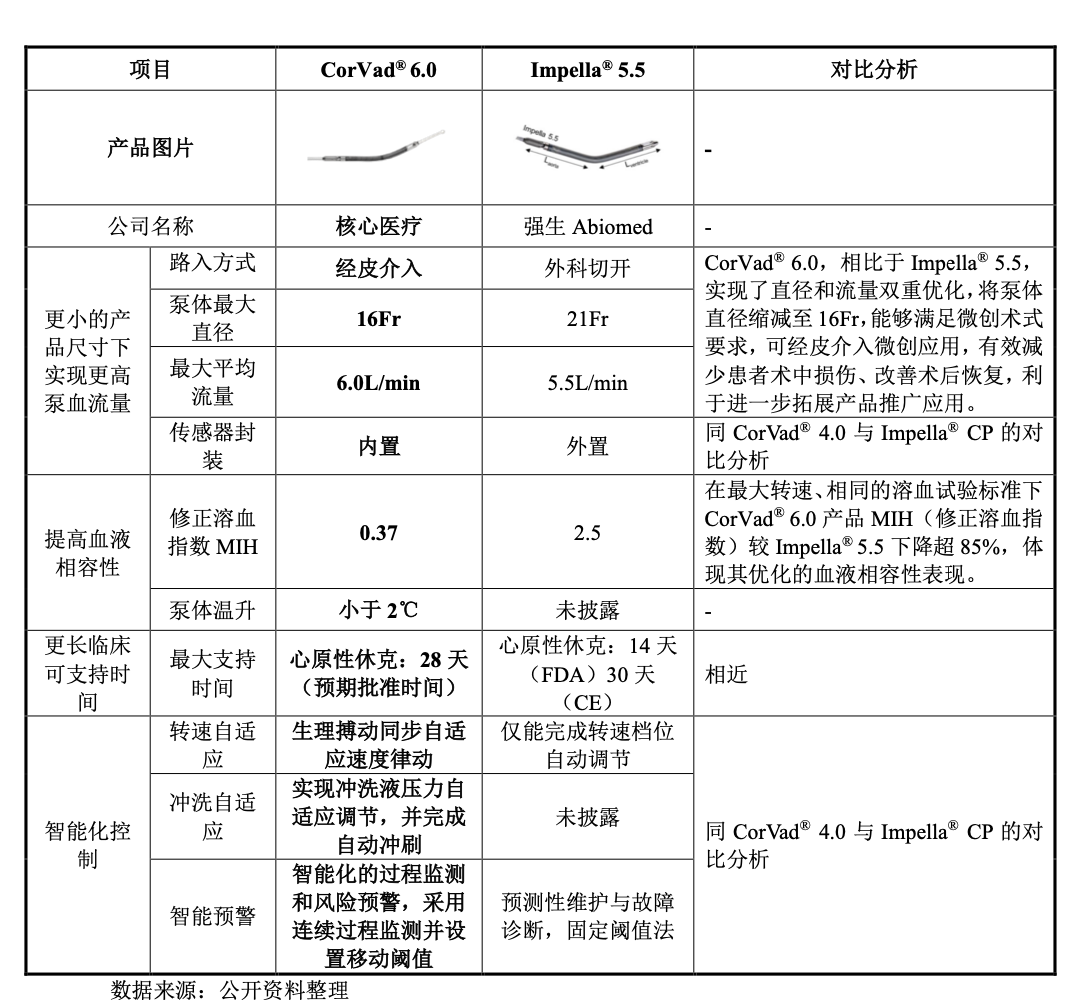
(图:介入式人工心脏CorVad® 6.0与Impella® 5.5对比分析)
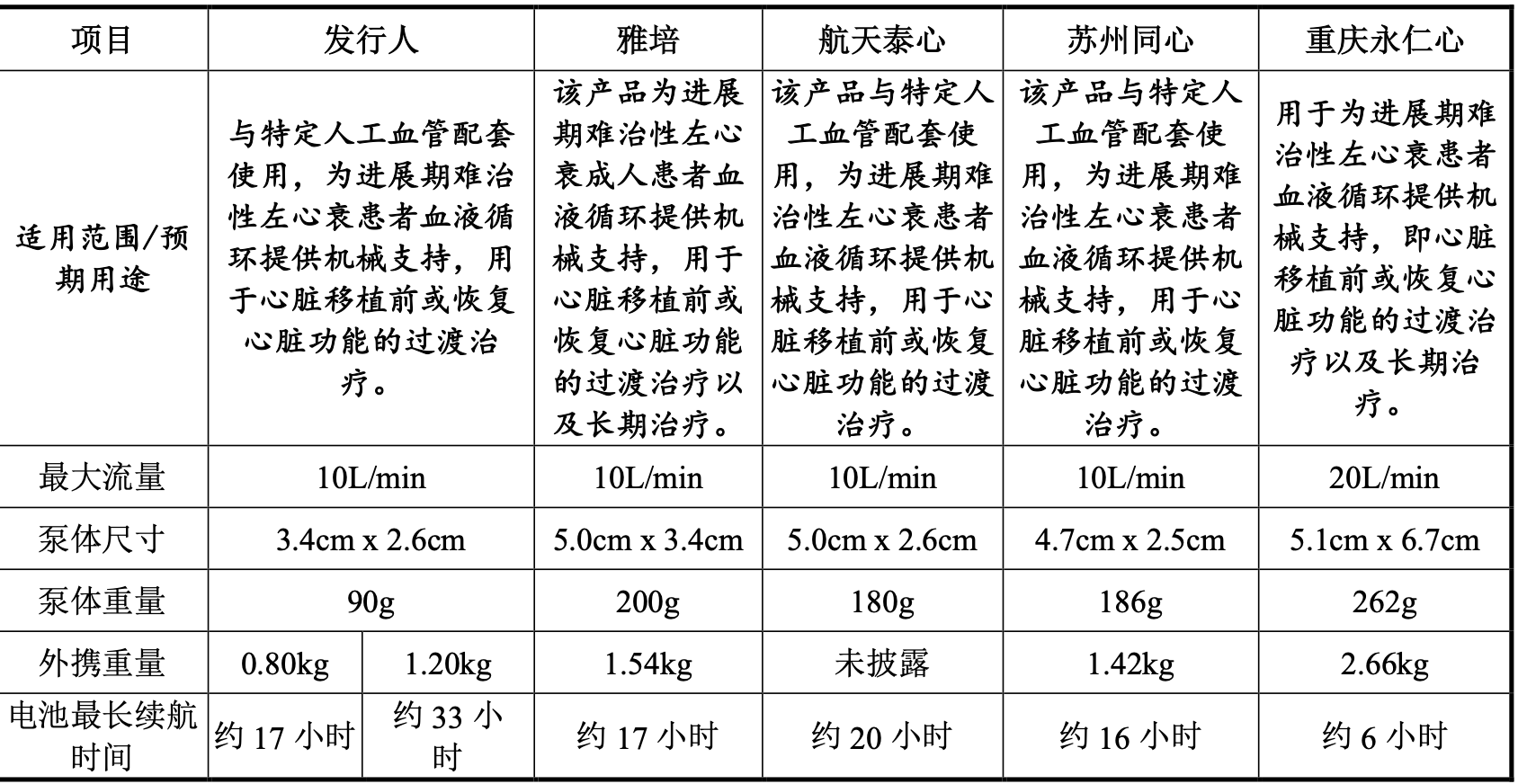
与雅培、航天泰心、苏州同心、重庆永仁心四家同行业可比公司的产品相比,核心医疗Corheart® 6的最大流量与国内外主流产品差异不大,但泵体尺寸、泵体重量、外携重量三大指标均为其可比产品中最优;而Corheart® 6的电池最长续航时间约17小时,属于中间水平。

截至目前,核心医疗的其他在研项目包括,针对终末期全心衰的磁悬浮双心辅助系统DuoCor2、针对幼儿心衰的幼儿心室辅助系统CorheartKid、针对进展期急性心衰的经心尖微创左心室辅助系统CorheartBTR,上述三大项目或均有望成为全球范围内首发获批产品。
其中,DuoCor2于2024年11月进入我国创新医疗器械审查程序,已进入临床评价阶段,在欧洲已启动临床试验。截至本回复出具日,DuoCor2亦为我国唯一进入创新医疗器械审查程序的双心辅助系统,并有望成为全球范围内首款获批的植入式双心辅助系统,其预计2027年于国内及欧洲递交注册申请,具备显著先发优势。
CorheartKid和CorheartBTR尚未进入临床评价阶段,预计2029年获批。
根据核心医疗的说法,截至本回复出具日,我国范围尚无儿童专用的已上市植入式人工心脏,全球范围亦无可适用于婴幼儿的已上市全磁悬浮植入式人工心脏。Corheart® Kid作为专门针对低龄、低体重终末期心衰患儿设计的植入式人工心脏,有望填补终末期低龄、低体重儿童心衰领域的治疗空白,临床价值凸显。
此外,全球范围尚未与Corheart® BTR相同应用场景的同类植入式人工心脏产品获批上市。相较于传统植入式人工心脏和介入式人工心脏,Corheart® BTR巧妙结合了植入式人工心脏的长期可靠性与介入式人工心脏的微创性两大核心优势,为患者提供了一种过渡性治疗方案。
与多家大学、医院联合研发儿童专用心室辅助装置
值得一提的是,从人工心脏领域适应症和未来重点应用来看,上交所还在审核问询中提及核心医疗对于对于长期治疗适应证申请和儿童专用心室辅助装置的研发及国产化项目。
核心医疗对此回复表示,国内已上市的5款植入式人工心脏均己获批过渡治疗适应证,其中重庆永仁心的EVAHEART®与雅培的HeartMate3同时获批了过渡治疗和长期治疗两种适应证。
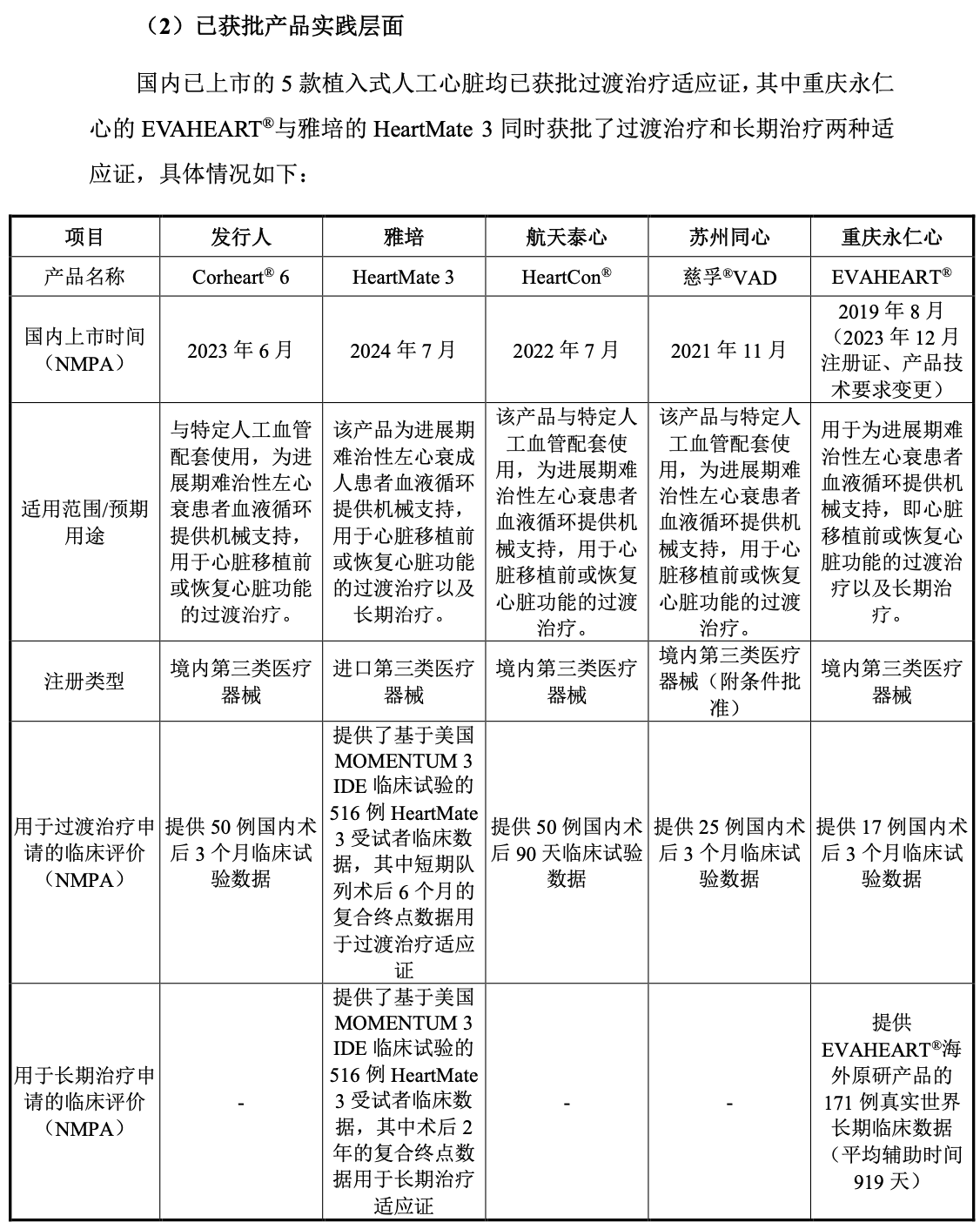
核心医疗已获批非长期治疗系统的适用范围,拟申报用于长期治疗系统的适用范围。不过,鉴于相关文件目前尚处于征求意见稿阶段,其相关要求的最终施行标准及时间存在不确定性。
核心医疗现有两项长期临床研究正在开展。
一是Corheart® 6注册临床试验长期随访延长研究,预计将于2027年完成5年长期随访工作,受试者植入后24个月的临床数据现已完成数据清理及统计分析,长期临床数据已公布;二是Corheart® 6大样本真实世界长期队列研究:目前正在积极开展,相关随访数据正处于持续收集整理中。
儿童专用心室辅助装置的研发及国产化方面,核心医疗于2023年与华中科技大学、上海儿童医学中心等6家医院合作进行相关研发,2024年与华中科技大学附属医院合作进行植入式双心室辅助系统的相关临床研究,合作研发形成1项共有专利“双心室辅助系统的转速自适应方法及装置”。
核心医疗还承担了“十四五”国家重点研发计划项目“儿童终末期心衰临床关键技术突破及诊疗规范建立”和2025年度国家科技重大专项“复杂冠心病早期风险预测及诊疗新策略研究”。
2025年上半年Corheart® 6产销率为83.65%
根据回复文件,核心医疗构建了涵盖植入式与介入式的完整产品矩阵,全面覆盖“长期→短期、左心→双心、幼儿→成人”的临床需求。核心医疗首款商业化产品Corheart® 6进展较快,根据相关公开数据来源,2024年度Corheart® 6终端植入量市占率超45%,位居行业第一。
最新数据显示,2025年上半年,Corheart® 6的产量为367台,销量为307台,产销率为83.65%,相较于2024年度94.04%的产销率有所下降。但其72.09%的主营业务毛利率较2024年度有所提升,6.41万元/台的单位成本相较于2024年同期数据则有所下降;2025年上半年的综合毛利率为72.09%,略高于同行业可比公司70.68%的平均值。
市场空间方面,根据弗若斯特沙利文预测,2024年全球植入式人工心脏植入量为7538台,其中美国植入量为3919台,占比51.99%;欧洲植入量为2117台,占比28.08%;中国植入量为748台,占比为9.92%,前述三者合计占比为90%,系植入式人工心脏产品的主要应用市场。
根据弗若斯特沙利文预测,中国的植入式人工心脏年植入量将维持高速增长态势,2033年预计达25087台,对应2024-2033年预计复合年增长率达47.7%;预计到2033年,中国市场将成为全球最主要的植入式人工心脏市场,年植入量占全球比例预计可达39.97%。
全球市场方面,2024年全球心衰患者数量为6298.1万人,预计到2033年将增加至7151.1万人,预计复合年增长率1.4%。其中2024年终末期心衰患者为605.9万人,预计2033年将达到647.4万人,2024年至2033年复合年增长率为0.7%。


