在BNT162b2的好消息宣布后,复星董事长郭广昌也随即发声,“这次我们合作研发的mRNA疫苗有效率高达90%,而普通流感疫苗也只有70%左右的保护率,远超我们此前的预期,更远远高于FDA要求的50%以上即可获批上市。”

《科创板日报》(上海,记者 朱洁琰)讯,周一美股盘前,辉瑞和BioNTech宣布其合作研发新冠疫苗的保护效力达到90%以上,欧美股市、原油等风险资产应声狂飙。
这则消息之所以能够引爆全球金融市场,是因为结果远超预期。辉瑞和BioNTech的候选新冠疫苗BNT162b2的III期临床中期分析数据显示,该临床共入组了4.4万人,在接种完整剂次疫苗7天之后,该疫苗的保护效力达到90%以上,大幅超出此前美国FDA定的50%。
除此之外,在安全性上,本次试验没有发生严重不良反应,后续将继续收集有关安全性的数据。
当达到FDA要求的安全性评价要求之后(中位随访时间达到2个月),辉瑞和BioNTech将尽快提交紧急使用授权(EUA),时间预计是在11月的第三周。
目前,该III期临床将继续进行,在达到164个COVID-19病例的时候将进行最终的数据分析,并获得进一步的信息。
关于该疫苗的生产,辉瑞和BioNTech预计今年可以生产5000万剂次,2021年可以生产13亿剂次。
受该消息刺激,截至发稿,辉瑞上涨超7%,BioNTech上涨超13%。
今年3月15日,复星医药宣布获BioNTech许可在中国独家开发和商业化基于其mRNA技术平台研发的针对COVID-19的疫苗产品。3月17日,辉瑞宣布与BioNTech签署共同开发和分销基于mRNA的冠状病毒疫苗的意向书,面向除中国以外的市场。
这也就是说,复星医药是BioNTech在中国的合作伙伴,辉瑞是海外的合作伙伴。
BioNTech旗下mRNA新冠候选疫苗一共有四款。除此次宣布重磅利好的BNT162b2,复星医药与BioNTtech合作研发的BNT162b1在国内的I期临床试验的144例受试者也已于9月4日全部完成间隔21天的两次免疫接种,目前反应良好。
复星医药方面表示,正在积极与监管部门沟通,力争尽快在国内启动BNT162b2的临床试验。
复星内部人士还告诉《科创板日报》记者,复星持有BioNTech四款mRNA新冠候选疫苗中国区的全部权益。
在BNT162b2的好消息宣布后,复星董事长郭广昌也随即发声,“刚刚获悉一个好消息,复星新冠疫苗在全球的研发合作伙伴辉瑞和BioNTech刚刚宣布,根据三期临床试验的初步分析数据,这次我们合作研发的mRNA疫苗有效率高达90%,而普通流感疫苗也只有70%左右的保护率,远超我们此前的预期,更远远高于FDA要求的50%以上即可获批上市。”
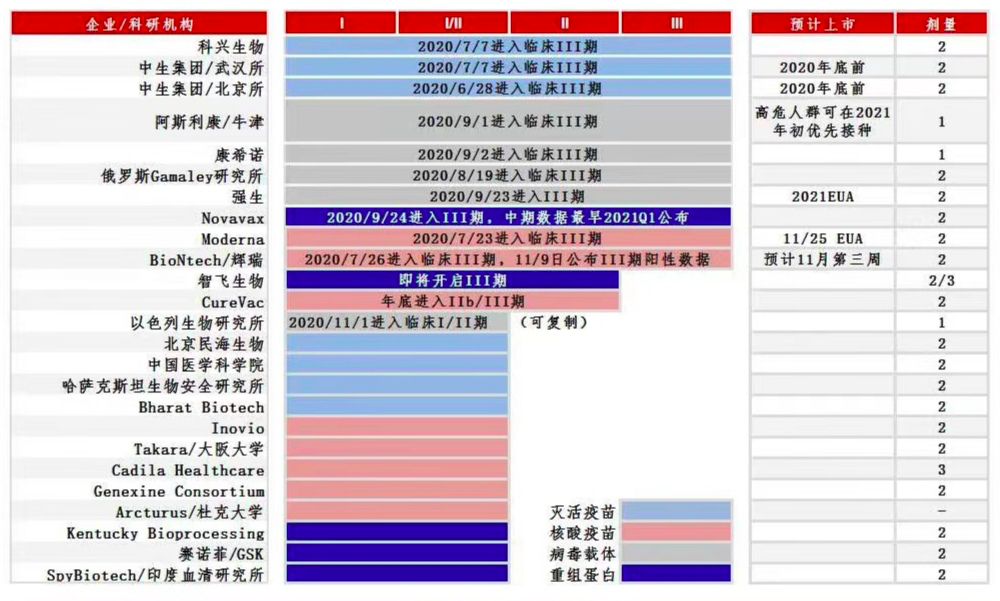
据国盛证券梳理,目前已有明确预估上市时间表的新冠疫苗研发企业还有阿斯利康、强生、Moderna,国内是中生集团/武汉所、中生集团/北京所。