

①在生物医药与生物制造两大万亿级市场中,MoleculeOS已具备解决AlphaFold 3等现有模型尚未完全攻克的复杂场景能力; ②该平台已在生物医药、合成生物学和新材料开发等领域实现落地; ③AI正颠覆创新药研发的“双十定律”。

《科创板日报》2月6日讯(编辑 宋子乔) AI能为蛋白质设计提供多少助力?
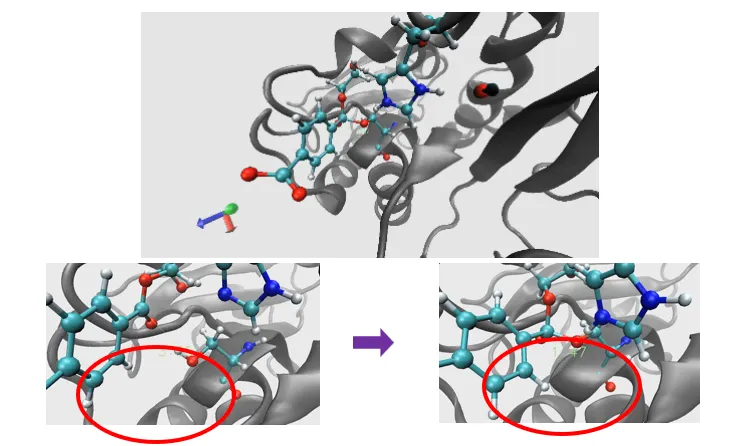
近日,分子之心宣布其AI蛋白质优化与设计平台MoleculeOS完成重大代际升级,在特定工业级应用场景下取得了突破性进展,解决了AlphaFold 3等模型无法解决的产业难题。例如,针对蛋白质动态结构预测与蛋白质动态设计的难题,分子之心融合AI、分子动力学与第一性原理方法,建立了高精度分子建模体系,能够高效模拟蛋白在不同环境条件下的构象变化和功能响应,在保持精度与传统量子化学方法一致的前提下,运行效率较其提升了千亿倍,达到“工业可用”的水平。
这意味着,在生物医药与生物制造两大万亿级市场中,MoleculeOS已具备解决AlphaFold 3等现有模型尚未完全攻克的复杂场景能力。
目前,MoleculeOS已在数十家头部药企及合成生物学龙头的真实管线中验证了其产业价值:
与凯赛生物的合作,改造一个重要酶蛋白结构,使菌种产率相对于野生菌提高了5倍;
将一款因表达量低濒临放弃的融合蛋白药物,表达量提升超400倍,单体含量超90%,重新挽救其开发前景;
2个月交付客户用传统高通量筛选无法解决的pH敏感性药物设计难题,实现了pH 7.4与pH 6.0环境下的60倍超高亲和力差值。
分子之心成立于2022年,致力于用AI技术,将耗时漫长、成本高昂、成功率低的传统蛋白质研发过程,转变为可预测、可编程、高效率的工程化流程,以解决生物医药和生物制造等领域对理想功能性蛋白质的巨大需求。
该公司创始人许锦波被业界誉为“AI蛋白质折叠奠基人”。早在2016年,他开发的RaptorX-Contact方法,首次证明了深度学习能大幅提升蛋白质结构预测精度,为后来DeepMind的AlphaFold算法奠定了基础。“我们不是要让生物学家变成AI专家,而是要让AI成为每个生物学家都触手可及的超级工具。” 许锦波表示。
作为分子之心自主研发的产业级AI蛋白质基础设施平台,MoleculeOS以全球首个多模态AI蛋白质基础大模型NewOrigin(达尔文)为基座,已提供针对新药设计、酶优化等数十种具体解决方案,并能通过对话式AI让生物学家直接使用。NewOrigin由分子之心自研,面向分子设计而非单一预测任务进行训练,具备跨任务、跨行业复用能力。
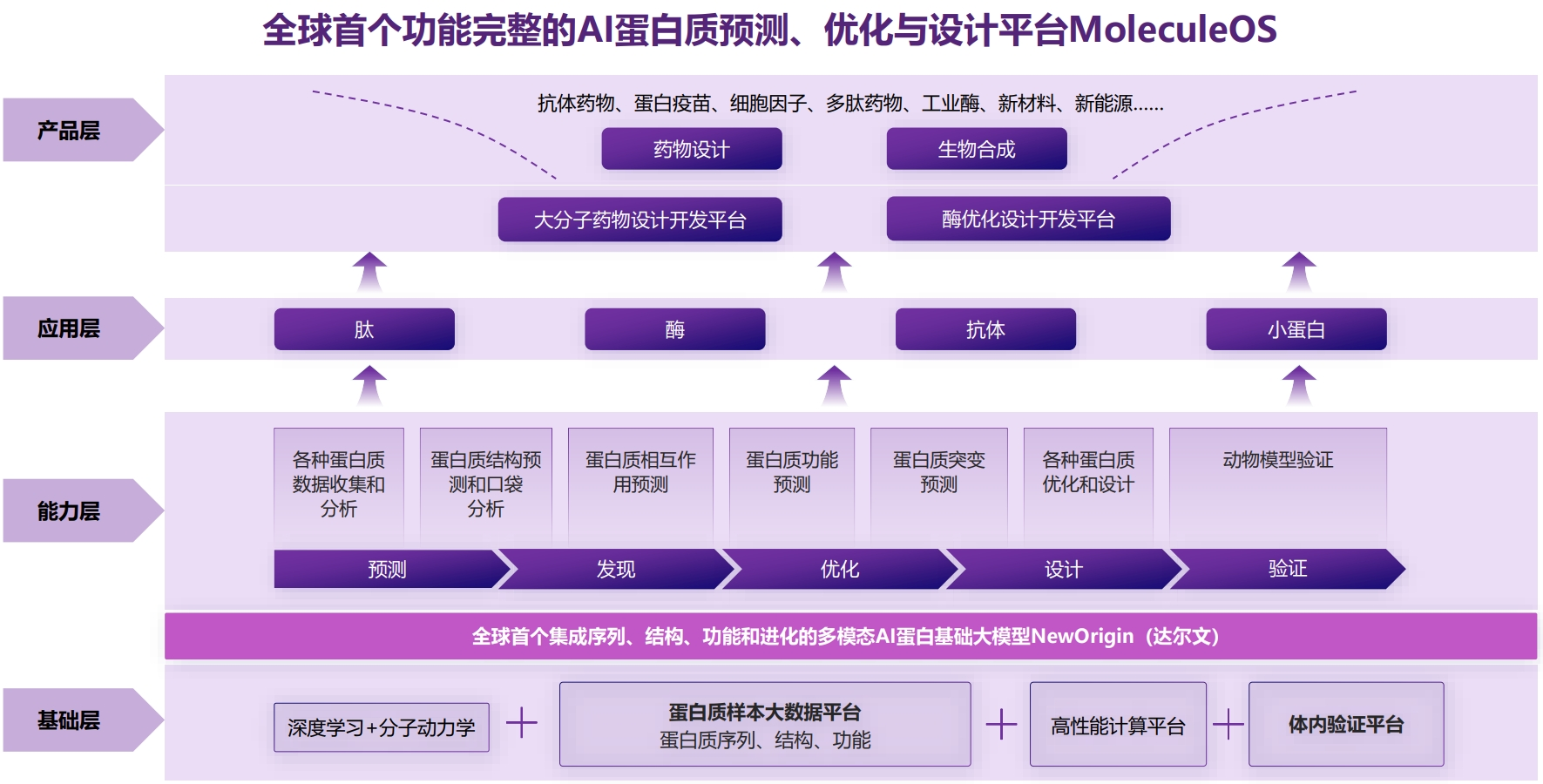
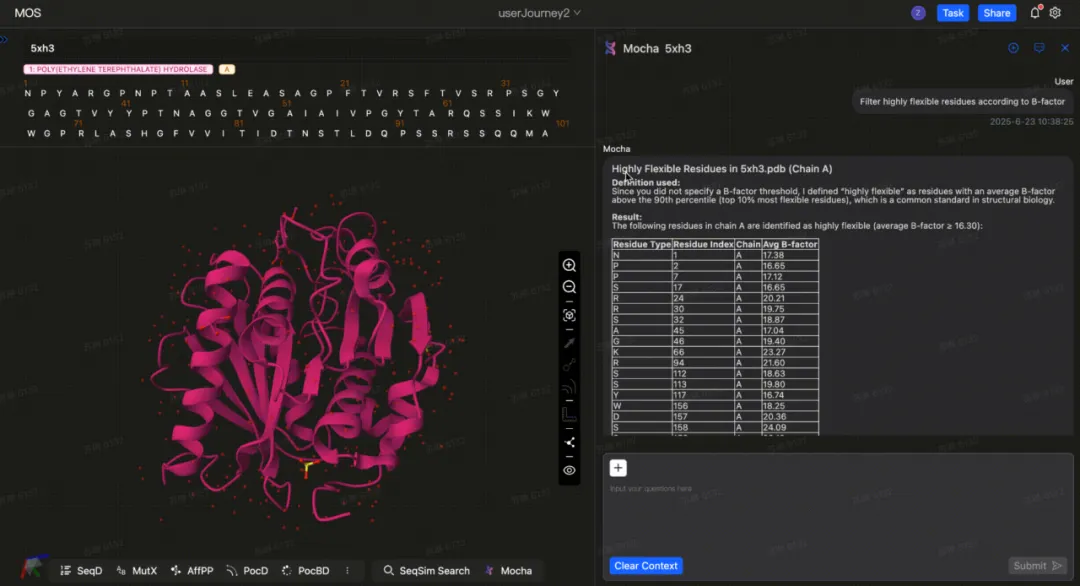
蛋白质设计是生物制药与生物制造的核心痛点,根本原因在于它处于整个研发流程的最上游和最高风险环节,其传统方法固有的高度不确定性、漫长周期和高昂成本直接向下游传导,形成了行业根本性瓶颈。
在传统的蛋白质设计与新药研发中,科学家们长期依赖于实验室试错。这个过程如同大海捞针,不仅耗费巨大的时间和成本,而且成功率微乎其微。这也导致了“双十定律”(十年研发、十亿美元投入)成为笼罩整个创新药领域的巨大魔咒。
而今,人工智能正在颠覆这一困局。AI蛋白质设计正将这一过程从“实验试错”转向“计算模拟与智能设计”。通过计算在数字世界中近乎无限地筛选和优化,仅对最有潜力的少数候选分子进行实验验证,从而直接攻击了上述三个痛点的根源,有望从根本上提升行业效率,将研究人员从漫长而繁重的实验操作中解放出来,使其能够更专注于核心目标的设定与成果分析。这种变革不仅大幅压缩了研发周期,也显著提升了成功率。