①中无人机近期称,该公司2025年经营规模较上年或有大幅增长,预计实现扭亏为盈;且军贸业务预计逐年增长;
②中无人机军贸业务占比超80%。受此属性因素影响的客户依赖度和业绩波动性亦较大。
编者按:
为帮助投资者更好了解企业真实发展情况与价值,进一步保护投资者合法权益等,财联社、《科创板日报》联合打造《直击股东会》栏目。
《直击股东会》栏目以现场报道的形式,通过在股东会现场直面上市公司董事长等核心管理层,聚焦企业长期战略、重大决策、经营方针等,旨在提升企业资本市场形象,优化投资者关系管理,完善上市公司相关治理与发展等。
本期企业
欧林生物
▍企业简介
欧林生物是一家专注于人用疫苗研发、生产及销售的生物制药企业,成立于2009年,致力于技术创新和产品研发,聚焦于“超级细菌”系列疫苗以及“成人疫苗”,形成了“阶梯有序、重点突破、多产品储备”的产品研发格局。
▍企业亮点
欧林生物是目前国内已知在“超级细菌”疫苗领域布局最为完善的疫苗企业,围绕WHO公布的“12种最危险的耐药细菌名单”,对重组金葡菌疫苗、口服重组幽门螺杆菌疫苗(大肠杆菌)、重组铜绿假单胞菌疫苗、重组鲍曼不动杆菌蛋白疫苗等“超级细菌”疫苗进行研究,均为全球1.1类新药。
▍盈利模式
欧林生物目前已实现3个产品上市销售,包括吸附破伤风疫苗、b型流感嗜血杆菌结合疫苗和A群C群脑膜炎球菌多糖结合疫苗。其中,公司吸附破伤风疫苗国内市场占有率多年处于行业领先地位。
《科创板日报》4月23日讯(记者 黄修眉) 欧林生物近日召开2024年度股东大会,审议并通过了《关于公司2024年度董事会工作报告的议案》《2024年年度利润分配方案的议案》等总共9项议案。

2024年吸附破伤风疫苗收入占比超90%
欧林生物2024年报显示,该公司实现营收5.89亿元,同比增长18.7%;实现归母净利润2076万元,同比增长18.2%。其去年营收创下2017年以来最高值。

(欧林生物各报告期营收情况)
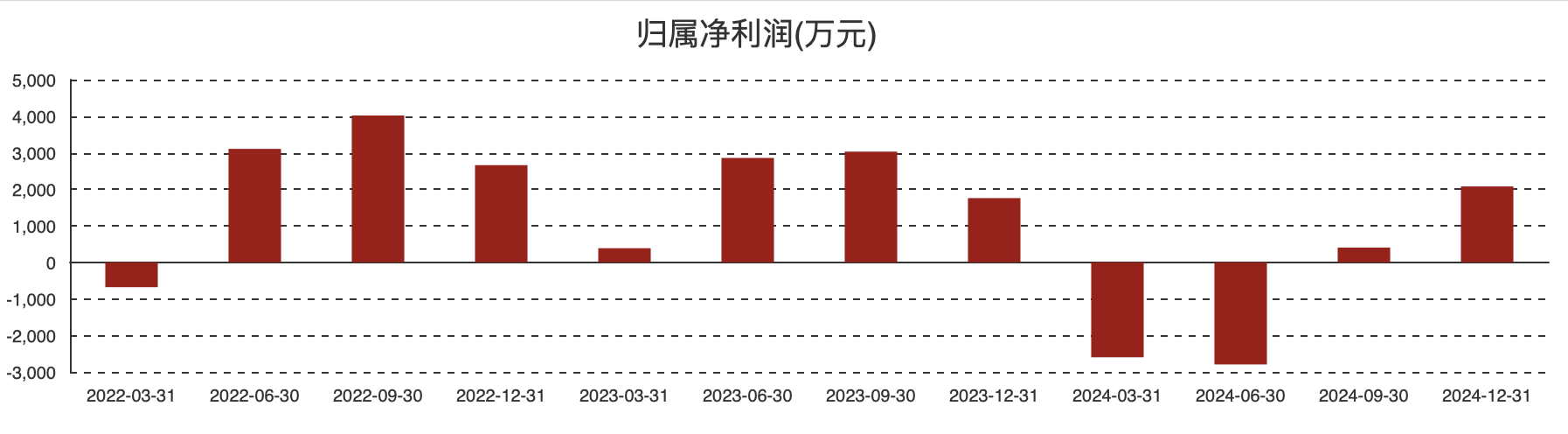
(欧林生物各报告期归母净利润情况)
据欧林生物介绍,该公司是国内第一家生产、销售吸附破伤风疫苗的民营企业。吸附破伤风疫苗是欧林生物2017年6月上市销售的首个产品。
欧林生物在2024年报中表示,公司吸附破伤风疫苗的销售实现稳健增长,单产品年销售收入首次突破5亿元,达5.358亿元,同比增长15.7%,占2024年度总营收比例90.99%。
从过往销售数据来看,欧林生物核心产品吸附破伤风疫苗收入持续增加。2019年至2023年各期期末,该公司核心产品吸附破伤风疫苗营收分别为1.3亿元、2.91亿元、3.93亿元、4.38亿元、4.63亿元,占当期公司总营收比重分别为72.57%、90.94%、80.6%、79.94%、93.32%。近年来,其单品收入与总营收占比均有所升高。
对于吸附破伤风疫苗占营收规模较高及未来市场增长潜力等问题,欧林生物相关负责人向《科创板日报》记者表示,“吸附破伤风疫苗接种需求主要有三种:一是被猫狗等咬伤,疾控中心通常会建议狂犬疫苗联合破伤风疫苗接种;二是日常生活和工作中的损伤等伤口感染风险;三是少部分为血液制品客户需求。”
“根据我们的测算,到2030年,狂犬疫苗接种人群和破伤风被动免疫患者市场渗透率分别为10%和30%,但目前渗透率远不及该数字,因此市场需求仍有较大的增长空间。”上述负责人表示。
预计2027年首款“超级细菌”疫苗将量产
《科创板日报》记者注意到,近年来,欧林生物在吸附破伤风疫苗为营收主力的基础上,积极布局病毒领域和超级细菌领域。在当天举行的2024年度股东大会上,有投资者重点问及该公司“超级细菌”领域疫苗的研发进展。
在临床领域,细菌耐药性是一个亟待解决的空白问题。欧林生物围绕2017年WHO公布的“12种最危险的耐药细菌名单”,布局了重组金葡菌疫苗、口服重组幽门螺杆菌疫苗(大肠杆菌)、重组铜绿假单胞菌疫苗、重组鲍曼不动杆菌蛋白疫苗等四类原创“超级细菌”疫苗,均为全球1.1类新药。
根据欧林生物2024年报的披露,该公司重组金黄色葡萄球菌疫苗的Ⅲ期临床试验计划入组人数为6000例,截至2024年底已完成入组5000余例。
欧林生物相关负责人表示,“根据规划,今年6月,上述6000组临床试验将完成入组,此后将经过约180天的安全观察期。Ⅲ期临床试验数据结果预计将在2026年上半年左右完成,此后该疫苗会经历上报审批、流程检查、工艺生产等多个环节,预计初步量产时间在2027年左右。”
需要注意的是,截至目前,全球范围内暂未有成功获批上市的金葡菌疫苗,国内仅有欧林生物进入临床试验阶段。
从经济效益来看,欧林生物实控人之一、副董事长樊钒曾透露,据预估,我国医院住院手术病人超5000万人次/年,目前手术病人金葡菌感染率为5%-8%,按术后抗生素与静注人免疫球蛋白联合给药方法推算,仅这一市场理论规模便将超过百亿元。
除此之外,2024年6月4日,欧林生物发布关于自愿披露口服重组幽门螺杆菌疫苗(大肠杆菌)在澳大利亚获得I期临床试验许可的公告。
“我们的幽门螺杆菌疫苗目前暂未开展临床试验。一是希望对疫苗进行升级,二是公司还是希望能在明年于国内进行试验申报。”上述相关负责人表示,“从幽门螺杆菌的感染率和适用范围来看,在国内进行临床试验的准确率、适应率等应该会更高。”
中国疾控中心传染病预防控制所2023年6月发布《中国幽门螺杆菌感染防控》白皮书显示,我国居民幽门螺杆菌人群感染率近50%,不同人群感染率在35.4%-66.4%之间。这也就意味着一旦有公司生产出幽门螺杆菌疫苗,其将拥有非常广阔的潜在市场。
目前全球范围内对幽门螺杆菌疫苗的探索虽已取得诸多研究成果,但至今暂无任何疫苗产品在全球市场获得批准上市。


